Jiachang Biological - biotechnology services and research and development as one of the high-tech enterprises
High qualityefficienttransparent
High quality, efficient and transparent
發布時間:2022-12-14 16:22 信息來(lái)源: 閱讀(dú)次數: 次
人(rén)間充質幹細胞(human mesenchymal stem cells, hMSCs)是一類存在于不同組織間質或血管周圍、形态類似于成纖維細胞的成體(tǐ)幹細胞,可(kě)在體(tǐ)外自(zì)我更新并具有成骨、成脂、成軟骨等分(fēn)化能力。hMSCs具有獨特的、與治療疾病密切相(xiàng)關的生(shēng)物學有效性(biological effectiveness),因此已成爲臨床研究中發展最爲迅速的一類幹細胞,具有廣泛的臨床應用價值。
hMSCs質量屬性
臨床應用的hMSCs應具有四類質量屬性:基本細胞生(shēng)物學屬性,微生(shēng)物學安全性,生(shēng)物學安全性和生(shēng)物學有效性。其中生(shēng)物學有效性與hMSCs臨床治療效應密切相(xiàng)關,是臨床前研究階段用于預測臨床治療效應,是現階段乃至未來(lái)決定hMSCs臨床轉化是否能成功的重要質量屬性。不同組織來(lái)源的 hMSCs生(shēng)物學有效性質量屬性,可(kě)歸類爲誘導分(fēn)化功能、免疫調控能力及組織再生(shēng)功能,而每一類别中又含有細化的内容(或質量屬性)。
體(tǐ)外評價hMSCs細胞向不同譜系的分(fēn)化能力是hMSCs生(shēng)物學有效性質量評價的關鍵質量屬性,接下來(lái)就(jiù)hMSCs的生(shēng)物學有效性評價中的多向分(fēn)化潛能作(zuò)詳細介紹。
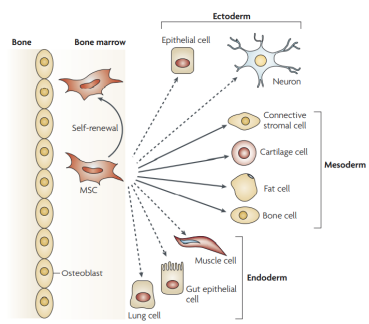
hMSCs多向分(fēn)化潛能及其檢測方法
hMSCs在特定體(tǐ)外誘導分(fēn)化培養條件(jiàn)下,具有向内、中、外胚層不同細胞系分(fēn)化的潛能。在體(tǐ)外質量評價實驗中,可(kě)以通過特定的誘導條件(jiàn)将hMSCs向特定功能細胞分(fēn)化,進而運用不同檢測技術(shù)對分(fēn)化細胞的相(xiàng)關生(shēng)物學特性或功能進行評價。目前普遍接受由ISCT于2006年(nián)首次提出的以成骨、成脂、成軟骨細胞誘導分(fēn)化能力的評價方法。
一、 hMSCs成骨細胞誘導分(fēn)化:
在體(tǐ)外培養條件(jiàn)下,經過特定誘導條件(jiàn)使hMSCs分(fēn)化發育爲成骨細胞。通常将這個分(fēn)化過程劃分(fēn)爲細胞增殖期、分(fēn)化早期、分(fēn)化中晚期三個階段。hMSCs 在貼壁後就(jiù)開始進入細胞增殖階段,以DNA複制和組蛋白(bái)合成爲特征。分(fēn)化早期則以堿性磷酸酶活性升高、I型膠原分(fēn)泌爲特征,同時還(hái)伴有細胞增殖抑制。分(fēn)化中晚期主要以鈣離(lí)子的沉積爲特征。故常通過檢測鈣離(lí)子沉澱“鈣結節”的量來(lái)表示成骨分(fēn)化的強弱。
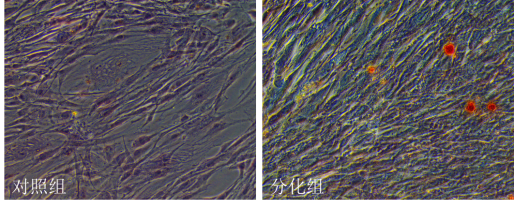
茜素紅(hóng)S是橙黃(huáng)色的針狀體(tǐ),由茜素經發煙硫酸磺化,然後轉變爲鈉鹽制得(de)。屬一種蒽醌(Anthraquinone)類的衍生(shēng)物,是茜素磺酸鈉鹽,它能與鈣鹽以鳌和方式形成橘紅(hóng)色複合物,用以識别組織細胞的鈣鹽成分(fēn)。經茜素紅(hóng)(alizarin red)染色呈陽性,提示成骨誘導分(fēn)化後細胞内可(kě)形成礦化基質。
二、 hMSCs成脂細胞誘導分(fēn)化:
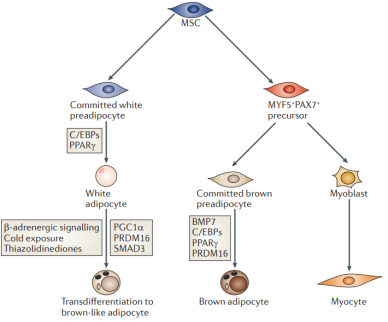
人(rén)和哺乳動物體(tǐ)内的脂肪組織可(kě)以分(fēn)爲白(bái)色脂肪組織和棕色脂肪組織,兩種脂肪組織的細胞中均含有脂肪,但(dàn)是他(tā)們在分(fēn)布位置和結構功能上有所區别。白(bái)色脂肪組織普遍分(fēn)布在皮下組織和内髒周圍,主要起能量倉庫的作(zuò)用,将多餘的能量以脂肪的形式儲存起來(lái)。棕色脂肪組織主要分(fēn)布在頸部兩側、背部上側、鎖骨附近和脊柱周圍,其細胞内含有大(dà)量線粒體(tǐ),可(kě)以将食物中的能量轉化爲熱(rè)能。
hMSCs在相(xiàng)關誘導分(fēn)化培養基培養14~28 d後,經油紅(hóng)O(oil red 0)染色爲陽性,根據脂肪組織細胞的特點:細胞漿中含有脂肪滴,可(kě)以通過油紅(hóng)O對細胞中脂肪滴染色。說(shuō)明分(fēn)化的細胞内形成脂滴。
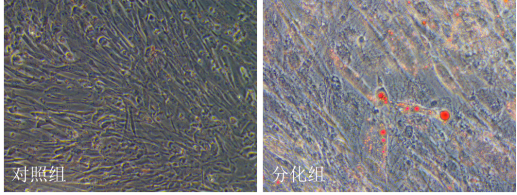
油紅(hóng)O(蘇丹紅(hóng))是一種脂溶性偶氮染料,能特異性地使組織和細胞内中性甘油三脂、脂質以及脂蛋白(bái)等染色。油紅(hóng) O 配成染色液用于染色時,可(kě)以通過相(xiàng)似相(xiàng)溶的原理(lǐ)使組織或細胞内的脂滴着紅(hóng)色,可(kě)用于分(fēn)析組織或細胞樣本中的脂質分(fēn)布情況。
三、 hMSCs成軟骨細胞誘導分(fēn)化:
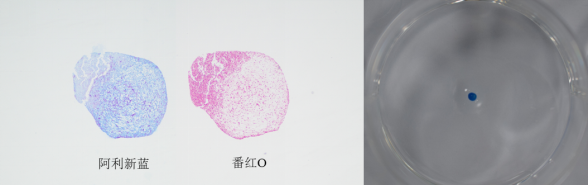
具有成軟骨分(fēn)化能力的hMSCs細胞在誘導培養過程中,可(kě)以自(zì)發收縮聚集形成細胞微球,并逐漸形成具有一定硬度和彈性并呈白(bái)色外觀的軟骨樣子組織。該組織經阿利新藍染色呈陽性。(在間充質幹細胞誘導分(fēn)化爲軟骨細胞後,細胞可(kě)以合成并分(fēn)泌大(dà)量細胞外基質,其中包括富含透明質酸的糖胺聚糖,可(kě)以被阿利新藍染成藍色。)伴随軟骨細胞分(fēn)化,Ⅱ型膠原等軟骨細胞特定基因表達水平會顯著上調,因此可(kě)利用在軟骨分(fēn)化條件(jiàn)下,hMSCs成細胞球能力、形成軟骨組織形态能力、番紅(hóng)O或阿新藍染色及軟骨特定基因表達上調情況綜合判斷hMSCs成軟骨細胞分(fēn)化能力。
這種基于三維細胞培養、形态學觀察和阿利新藍染色的檢測方法可(kě)以提供相(xiàng)對明确的成軟骨細胞分(fēn)化能力的信息。
相(xiàng)關法規指導
後台回複“幹細胞質量控制”,獲取相(xiàng)關指導文件(jiàn)。
武漢珈創生(shēng)物相(xiàng)關服務
金華海孚生物技術有限公司,創建于2011年(nián),是一家集生(shēng)物技術(shù)服務與研發爲一體(tǐ)的高新技術(shù)企業,專注于爲生(shēng)物藥品/制品的生(shēng)産企業及研發機(jī)構提供各類細胞(含重組細胞、幹細胞、免疫細胞等)及原輔料的質量檢測、病毒清除工(gōng)藝驗證技術(shù)服務。
質量檢測服務
武漢珈創生(shēng)物可(kě)按相(xiàng)關法規或者指導文件(jiàn)提供幹細胞治療産品的各個生(shēng)産環節的質量檢測服務,包括:
基本生(shēng)物學屬性檢測
細胞鑒别、細胞活性檢測、種屬間細胞污染的檢測、染色體(tǐ)核型分(fēn)析;
微生(shēng)物學安全性檢測
無菌檢測、支原體(tǐ)檢測,确保産品無微生(shēng)物污染或代謝産物污染;
生(shēng)物學安全性檢測
成瘤性和緻瘤性檢測、異常免疫反應檢測、殘留物的檢測;
生(shēng)物學有效性評價
多向分(fēn)化功能的評價、免疫調控功能的評價、hMSCs組織再生(shēng)功能的評價
幹細胞放(fàng)行快(kuài)檢
珈創生(shēng)物自(zì)主研發的放(fàng)行快(kuài)檢技術(shù),可(kě)在6小時内完成,涵蓋細菌、真菌和支原體(tǐ)快(kuài)檢技術(shù),且技術(shù)方法已成熟,經過了上百次驗證。
定制化服務
[1] Cristancho, A. G., & Lazar, M. A.(2011). Forming functional fat: a growing understanding of adipocytedifferentiation. Nat Rev Mol Cell Biol, 12(11), 722-734.https://doi.org/10.1038/nrm3198
[2] Dominici, M., Le Blanc, K., Mueller,I., Slaper-Cortenbach, I., Marini, F., Krause, D., . . . Horwitz, E. (2006).Minimal criteria for defining multipotent mesenchymal stromal cells. TheInternational Society for Cellular Therapy position statement. Cytotherapy,8(4), 315-317. https://doi.org/10.1080/14653240600855905
[3] Tang, N., Song, W. X., Luo, J., Haydon,R. C., & He, T. C. (2008). Osteosarcoma development and stem celldifferentiation. Clin Orthop Relat Res, 466(9), 2114-2130. https://doi.org/10.1007/s11999-008-0335-z
[4] Uccelli, A., Moretta, L., &Pistoia, V. (2008). Mesenchymal stem cells in health and disease. Nat RevImmunol, 8(9), 726-736. https://doi.org/10.1038/nri2395
[5] 周, 雷. (2017). Research Progress of Osteogenesis-Related SignalingPathways. Advances in Clinical Medicine, 07(04), 235-241.https://doi.org/10.12677/acm.2017.74039
[6] 關于印發幹細胞制劑質量控制及臨床前研究指導原則(試行)的通知,國(guó)家藥品監督管理(lǐ)局
[7] 張可(kě)華,劉靜(jìng),納濤,袁寶珠.人(rén)間充質幹細胞體(tǐ)外成軟骨分(fēn)化能力綜合評價策略研究[J].中國(guó)新藥雜志,2017,26(18):2196-2203.
[8] 韓曉燕,納濤,張可(kě)華,袁寶珠.人(rén)間充質幹細胞生(shēng)物學有效性的質量評價[J].中國(guó)新藥雜志,2018,27(21):2511-2518.

END