珈創生(shēng)物 —— 生(shēng)物技術(shù)服務與研發爲一體(tǐ)的高新技術(shù)企業
優質高效透明
High quality, efficient and transparent
發布時間:2022-04-06 18:06 信息來(lái)源: 閱讀(dú)次數: 次

每一篇藥典,都(dōu)是一部藥事(shì)寶典,它凝聚了無數醫藥人(rén)的智慧,是藥品研制、生(shēng)産、經營、使用和監督管理(lǐ)等均應遵循的法定依據。正因如(rú)此,藥典的内容通常會比較長,可(kě)能有小夥伴感覺閱讀(dú)起來(lái)挺費事(shì)兒?别急,小珈來(lái)爲您支招~
在咱們新開創的#藥典解讀(dú)#欄目裡(lǐ),小珈将持續用思維導圖幫大(dà)家梳理(lǐ)藥典思路(lù),盤點其重點内容,歡迎大(dà)家去(qù)後台留言探討(tǎo)。
本文解讀(dú)的是:《生(shēng)物制品病毒安全性控制》中華人(rén)民(mín)共和國(guó)藥典,2020年(nián)版,三部,生(shēng)物制品通則。
病毒安全性控制的意義
生(shēng)物制品在制備過程或制劑中,大(dà)概率會添加人(rén)或動物來(lái)源的原材料或輔料,這些原材料或輔料潛在的病毒污染是影(yǐng)響産品安全性的關鍵因素,因此需要控制生(shēng)物制品的病毒安全性風(fēng)險,以保證産品質量。
病毒安全性控制的原則
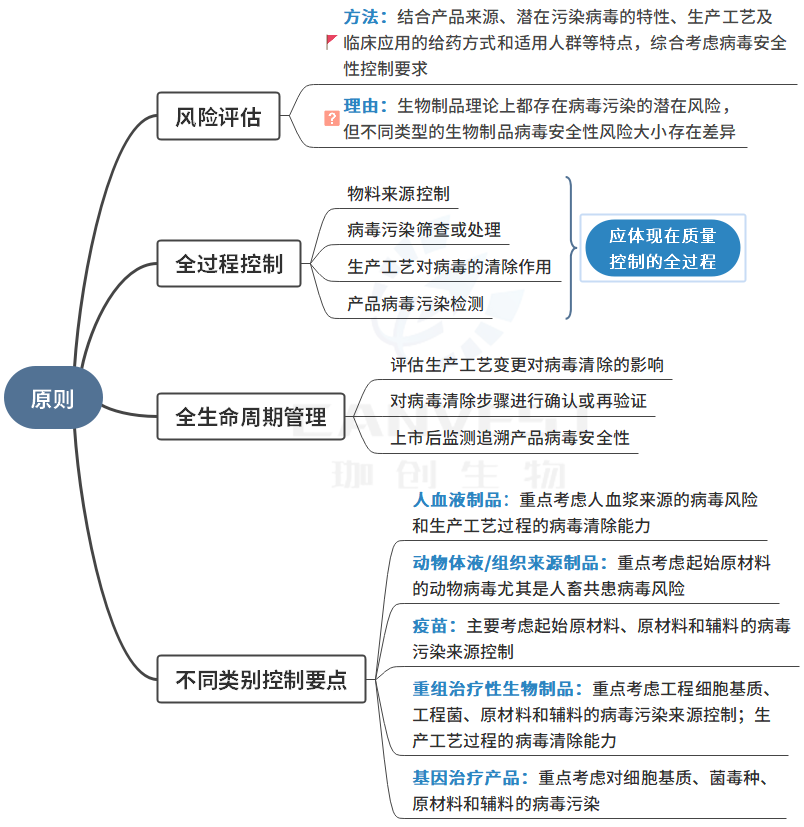
點擊看(kàn)大(dà)圖▲
病毒安全性控制要求
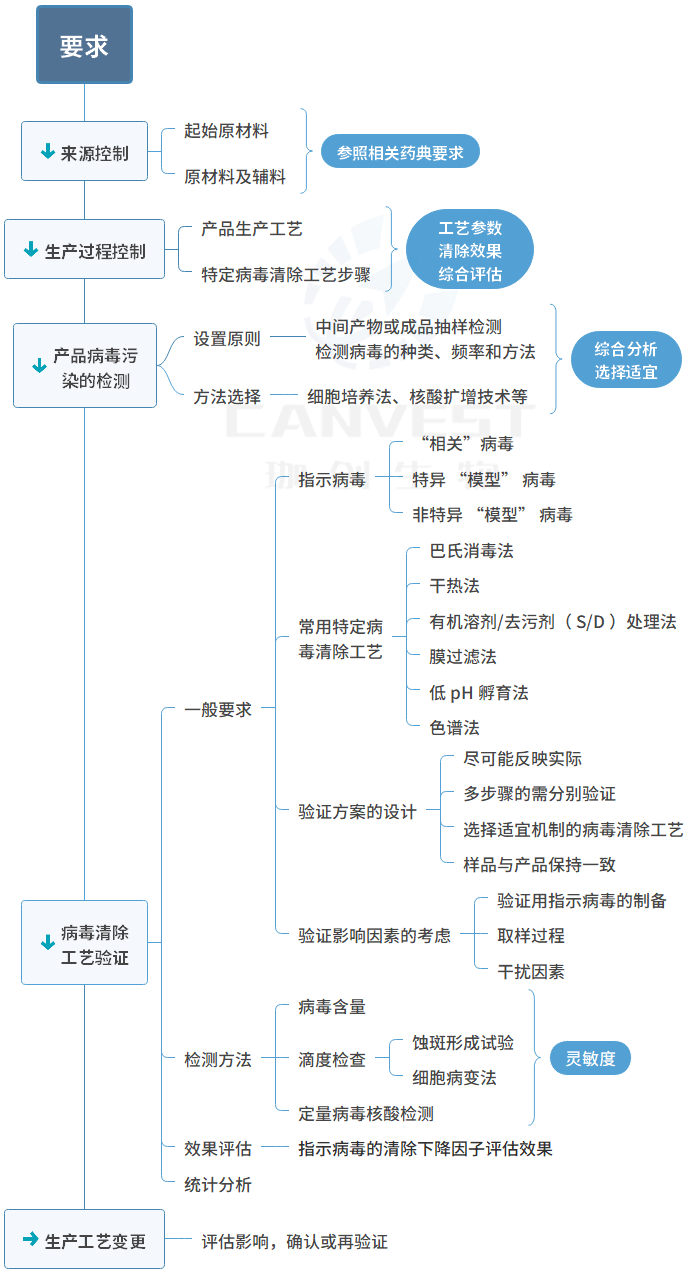
點擊看(kàn)大(dà)圖▲
來(lái)源控制
應參照(zhào)相(xiàng)關藥典要求,控制相(xiàng)應的起始原材料、原材料及輔料的病毒安全。
起始原材料
參照(zhào)藥典:生(shēng)産用細胞基質、菌毒種、血液制品生(shēng)産用原料血漿和動物體(tǐ)液/組織,應分(fēn)别符合“生(shēng)物制品生(shēng)産檢定用動物細胞基質制備及質量控制” “生(shēng)物制品生(shēng)産檢定用菌毒種管理(lǐ)及質量控制” “血液制品生(shēng)産用人(rén)血漿” “人(rén)用馬免疫血清制品總論” 及 “生(shēng)物制品生(shēng)産及檢定用實驗動物質量控制(通則 3601)” 。
原材料及輔料
參照(zhào)藥典:“生(shēng)物制品生(shēng)産用原材料及輔料質量控制”。
生(shēng)産過程控制
1. 産品生(shēng)産工(gōng)藝
應明确影(yǐng)響病毒清除效果的關鍵工(gōng)藝參數及控制範圍,并在此基礎上建立充分(fēn)的産品制備工(gōng)藝過程的控制策略。
2. 特定病毒清除工(gōng)藝步驟
根據潛在污染病毒的特性,結合産品特性和生(shēng)産工(gōng)藝、病毒清除工(gōng)藝的作(zuò)用機(jī)制和清除能力的綜合評估,選擇适宜的病毒清除工(gōng)藝。
病毒去(qù)除/滅活工(gōng)藝效果應經過驗證并符合相(xiàng)關要求。
應明确影(yǐng)響病毒清除效果的關鍵工(gōng)藝參數以及相(xiàng)應參數設定範圍對病毒清除效果的影(yǐng)響。
産品病毒污染的檢測
1. 病毒污染檢測原則
應綜合考慮多種因素對病毒污染檢測結果的影(yǐng)響,确定對生(shēng)産過程中的中間産物或成品進行取樣和檢測,以及應檢測病毒的種類、頻率和方法。
2. 病毒污染檢測方法的選擇
應結合品種特點和具體(tǐ)生(shēng)産情況綜合分(fēn)析,設計(jì)并選擇适宜的方法對潛在污染病毒進行檢測,應盡可(kě)能采用先進的技術(shù)和方法用于病毒污染的檢測。
病毒清除工(gōng)藝驗證
目的
證明實際生(shēng)産過程對病毒去(qù)除/滅活的有效性,并對病毒的整體(tǐ)降低水平作(zuò)出定量評估。
方法
在非生(shēng)産現場的特定實驗室進行,模拟實際生(shēng)産工(gōng)藝參數及控制條件(jiàn)下的處理(lǐ)過程,然後取樣測定經處理(lǐ)後産品中的殘留指示病毒。
重點考慮
指示病毒的選擇、選擇合适的特定病毒清除工(gōng)藝、驗證方案的設計(jì)、驗證影(yǐng)響因素的考慮、用于病毒清除研究的檢測方法、病毒清除效果的評估、适宜的統計(jì)分(fēn)析處理(lǐ)方法。
上市産品的病毒安全性追蹤
應定期對産品潛在病毒的污染進行回顧性追溯,采用适宜方法監測産品潛在污染病毒,實現上市後産品病毒安全可(kě)追溯。
珈創生(shēng)物病毒清除工(gōng)藝驗證服務優勢
金華海孚生物技術有限公司,創建于2011年(nián),是一家集生(shēng)物技術(shù)服務與研發爲一體(tǐ)的高新技術(shù)企業,專注于爲生(shēng)物藥品/制品的生(shēng)産企業及研發機(jī)構提供各類細胞(含重組細胞、幹細胞、免疫細胞等)及原輔料的質量檢測、病毒清除工(gōng)藝驗證技術(shù)服務。
公司實力
左右滑動查看(kàn)更多,點擊看(kàn)大(dà)圖
毒種優質:背景清楚,純度高,滴度可(kě)達8~9Log10/ml。
服務可(kě)靠:可(kě)驗證客戶下遊工(gōng)藝對病毒的去(qù)除/滅活效果,爲客戶提供定制的病毒清除工(gōng)藝驗證服務。
高效無憂:保證客戶驗證工(gōng)藝無障礙開展且60天(常規IND申報項目)即可(kě)完成相(xiàng)關驗證,并提供權威的檢測報告。
符合法規:依據中國(guó)藥典2020年(nián)版、國(guó)藥監注、國(guó)家食品藥品監督管理(lǐ)局、ICH、USP等相(xiàng)關要求進行技術(shù)服務,包括《生(shēng)物制品病毒安全性控制》、《動物源性醫療器械病毒滅活/去(qù)除有效性驗證的原則》、Viral Safety Evaluation of Biotechnology Products Derived from Cell Lines of Human or AnimalOrigin. 1999. ICH Q5A(R1)、Design, Evaluation, and Characterization of Viral Clearance Procedure.2016. USP General Chapter: <1050.1>等。
